20% de sulfadiazine + 4% d'injection de triméthoprime
Ingrédient actif
Sulfadiazine 20,00% p / v.
Triméthoprime 4,00% W / V
Action pharmacologique
La sulfadiazine est un médicament sulfa modérément efficace pour une utilisation systémique et est un agent bactériostatique à large spectre. Son mécanisme d'action est dû au fait qu'il est structurellement similaire à l'acide p-aminobenzoïque (PABA) et peut rivaliser avec le PABA pour agir sur la dihydrofolate synthase dans les bactéries, empêchant ainsi le PABA d'être utilisé comme matière première pour synthétiser la tétrahydrofolate requise par les bactéries, là-bas inhibant la synthèse de la protéine bactérienne jouent un effet antibactire.
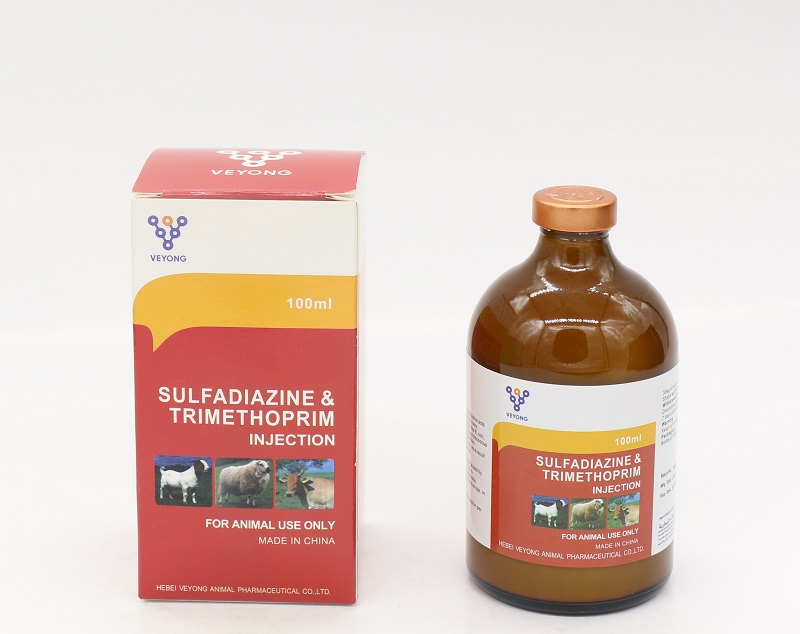
Indlcation
Cette solution injectable est indiquée dans le traitement des infections systémiques causées par ou associées à des organismes sensibles au triméthoprime: combinaison de sulfadiazine. Le spectre d'activité comprend à la fois des organismes Gram positifs et Gram-négatifs, notamment: Actinobacilli, Actinomycae, Bordetella spp, Brucella corynebacteria, Escherichia coli, Haemophilus spp. Klebsiella spp, Pasteurella spp, pneumocoque. Proteus, Salmonella spp. Staphylococci, streptocoques, vibrio.
Posologie et administration
Par injection sous-cutanée uniquement.
Bovins: Le débit de dose recommandé est de 15 mg d'ingrédients actifs par kg de poids corporel (1 ml par poids corporel de 16 kg) par injection intramusculaire ou lente intraveineuse.
Chevaux: Le débit de dose recommandé est de 15 mg d'ingrédients actifs par kg de poids corporel (1 ml par 16 kg de poids corporel), par injection intraveineuse lente.
Chiens et chats: Le taux de dose recommandé est de 30 mg d'ingrédients actifs par kg de poids corporel (1 ml par 8 kg de poids corporel).
Contre-indications
L'injection ne doit pas être donnée par des itinéraires autres que ceux recommandés.
À ne pas administrer par voie intrapéritonéale, intra - artérielle ou intrathécalement.
N'administrez pas aux animaux présentant une sensibilité connue au sulfonamide, des dommages parenchymateux hépatiques sévères ou des dyscrasies sanguins.
Avertissements spéciaux
1 Pour l'administration intraveineuse, le produit doit être réchauffé à la température corporelle et injecté lentement sur une période aussi longue que ce qui est raisonnablement pratique.
2 Au premier signe d'intolérance, l'injection doit être interrompue et le traitement du choc initié.
De l'eau potable adéquate devrait être disponible pendant l'effet thérapeutique du produit.
Période de retrait
Bovins: viande - 12 jours
Lait - 4 jours.
Stockage
Protéger de la lumière directe du soleil et stocker en dessous de 30 ℃.
Hebei Veyong Pharmaceutical Co., Ltd, a été créée en 2002, située dans la ville de Shijiazhuang, province de Hebei, en Chine, à côté de la capitale Pékin. Elle est une grande entreprise de médicaments vétérinaires certifiés GMP, avec R&D, production et ventes d'API vétérinaires, préparations, aliments prémélangés et additifs d'aliments. En tant que centre technique provincial, Veyong a créé un système de R&D innové pour de nouveaux médicaments vétérinaires et est l'entreprise vétérinaire technologique de renommée nationale, il existe 65 professionnels techniques. Veyong possède deux bases de production: Shijiazhuang et Ordos, dont la base de Shijiazhuang couvre une superficie de 78 706 m2, avec 13 produits API, notamment de l'ivermectine, de l'eprinoctine, du fumarate de tiamuline, de l'oxyttracycline Hydrochlory et désinfectant, ects. Veyong fournit des API, plus de 100 préparations d'étiquette et un service OEM et ODM.
Veyong attache une grande importance à la gestion du système EHS (environnement, santé et sécurité) et a obtenu les certificats ISO14001 et OHSAS18001. Veyong a été répertorié dans les entreprises industrielles émergentes stratégiques de la province du Hebei et peut assurer la fourniture continue de produits.

Veyong a créé le système complet de gestion de la qualité, a obtenu le certificat ISO9001, le certificat de GMP en Chine, le certificat GMP APVMA Australie, le certificat GMP de l'Éthiopie, le certificat d'ivermectine CEP et l'inspection de la FDA américaine. Veyong possède une équipe professionnelle d'inscription, de ventes et de services techniques, notre entreprise a obtenu sa dépendance et le soutien de nombreux clients par une excellente qualité de produit, des préventes de haute qualité et des services après-vente, une gestion sérieuse et scientifique. Veyong a fait une coopération à long terme avec de nombreuses entreprises pharmaceutiques animales connues internationales avec des produits exportés vers l'Europe, l'Amérique du Sud, le Moyen-Orient, l'Afrique, l'Asie, etc. Plus de 60 pays et régions.

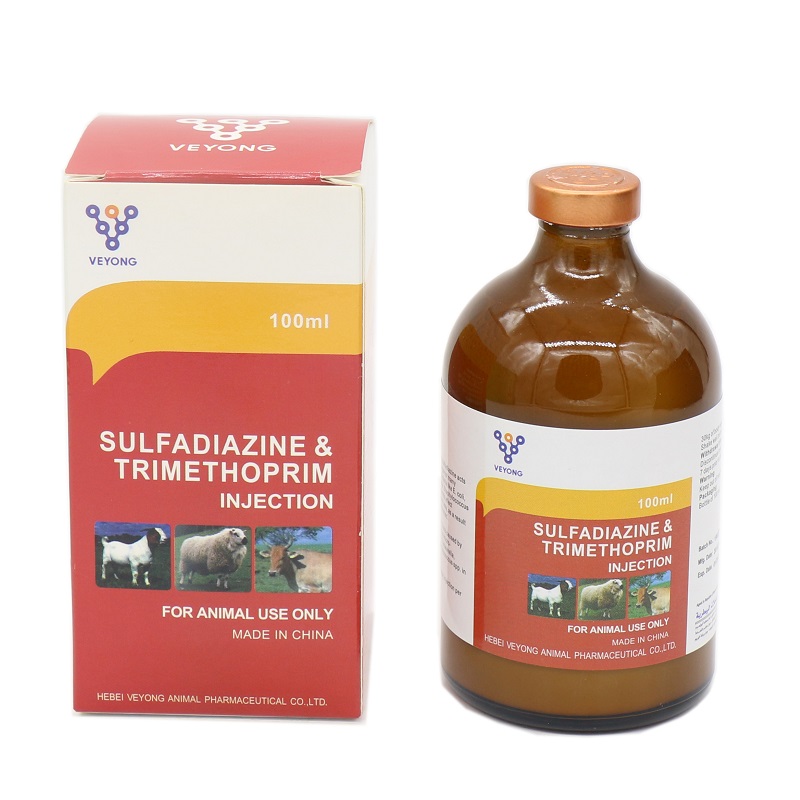



.png)
.png)
.png)
.png)